Molekulare Radioonkologie
In den letzten Jahrzehnten hat die Wissenschaft wichtige Kenntnisse über die Prozesse und Mechanismen in Krebszellen gewonnen. Auf Grundlage dieser Erkenntnisse wurden viele Therapien entwickelt. Strahlen- und Chemotherapie sind zwei der wichtigsten Strategien für die Behandlung von Patienten mit bösartigen Krebserkrankungen. Die Verbesserung der systemischen Chemotherapie führte zu Innovationen wie der zielgerichteten Therapie und der Immuntherapie, bei der die Krebszellen mit Antikörpern und niedermolekularen Kinaseinhibitoren (smKI) bekämpft werden. Darüber hinaus verbessert die moderne adjuvante Strahlentherapie die lokale Kontrolle und verringert die krebsspezifische Sterblichkeit. Um in der Krebstherapie weiter voranzukommen, wird die Kombination mehrerer verschiedener Therapien immer wichtiger, insbesondere im Rahmen der personalisierten Medizin. Wir erforschen dabei vielversprechende Kombinationen aus Strahlentherapie und Arzneimitteln, die auf krebsrelevante Signalwege abzielen, sowie ihr Potenzial zur gegenseitigen Beeinflussung bei verschiedenen hochrelevanten Entitäten wie Brustkrebs oder bei Kopf-Hals-Tumoren.
(Zahn-)Medizin Doktorand/-Innen
Katharina Wenkmann (IZKF gefördert)
Eva Schuhbaum
Optimierung der Behandlung des HNSCC durch Nutzung des radiosensibilisierenden Potenzials der zielgerichteten Therapie
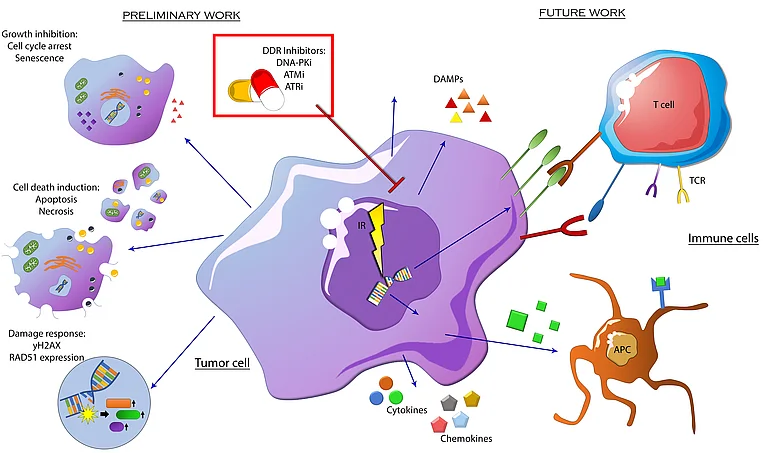
Die Strahlentherapie bzw. Radiotherapie (RT) ist eine präzise und lokal angewandte Behandlung, die häufig bei Tumoren in der Mundhöhle oder im Hypopharynx eingesetzt wird. Sie zielt darauf ab, DNA-Strangbrüche (DSB) in den Tumorzellen zu verursachen. Die gleichzeitige Verabreichung von Medikamenten (s.g. small molecule Kinase Inhibitoren, smKI) zur RT könnte dazu beitragen, die Effektivität der Strahlentherapie zu optimieren und gleichzeitig das Risiko in Bezug auf das Normalgewebe zu verringern. Diese Kombinationstherapie könnte dazu beitragen, das Risiko eines Therapieversagens bei z.B. Humanes Papilloma Virus (HPV)-negativem Plattenepithelkarzinom des Kopf-Hals-Bereichs (HNSCC) zu verringern und darüber hinaus eine Deeskalation der applizierten Dosis zum Schutz der Risikoorgane bei HNSCC zu ermöglichen. Das Forschungsfeld der Kombination von RT mit Kinase Inhibitoren gewinnt dabei weiter an Relevanz, da in den letzten Jahren viele neue Zielstrukturen in Tumorzellen (z.B. mutierte Proteine) identifiziert und daran bindende Inhibitoren entwickelt und zugelassen wurden. Da es allerdings immer noch an umfangreichen Daten über die Wechselwirkung von RT mit den meisten der zugelassenen smKI mangelt, haben wir den Einfluss mehrerer Inhibitoren, die von der EMA zugelassen sind oder derzeit in klinischen Studien geprüft werden, in Kombination mit RT untersucht und bereits viele additive und synergistische Wechselwirkungen identifiziert.
Ausgewählte Publikationen
Jost, T., Wachter, M., Meidenbauer, J., Fietkau, R., & Gaipl, U. S. Inhibiting the DNA damage repair of HNSCC cells in combination with normo-fractionated radiotherapy influences clonogenicity, senescence and expression of NK cell activation markers. Sci Rep. 2025;15(1):31827. Published 2025 Aug 29. doi:10.1038/s41598-025-17858-6
Meidenbauer, J., Wachter, M., Schulz, S. R., Mostafa, N., Zülch, L., Frey, B., Fietkau, R., Gaipl, U. S., & Jost, T. Inhibition of ATM or ATR in combination with hypo-fractionated radiotherapy leads to a different immunophenotype on transcript and protein level in HNSCC. Front Oncol. 2024;14:1460150. Published 2024 Oct 1. doi:10.3389/fonc.2024.1460150
Jost, T., Schuster, B., Heinzerling, L., Weissmann, T., Fietkau, R., Distel, L. V., & Hecht, M. (2022). Kinase inhibitors increase individual radiation sensitivity in normal cells of cancer patients. Strahlentherapie und Onkologie : Organ der Deutschen Rontgengesellschaft ... [et al], 198(9), 838–848. https://doi.org/10.1007/s00066-022-01945-y
Scheper, J., Hildebrand, L. S., Faulhaber, E. M., Deloch, L., Gaipl, U. S., Symank, J., Fietkau, R., Distel, L. V., Hecht, M., & Jost, T. (2022). Tumor-specific radiosensitizing effect of the ATM inhibitor AZD0156 in melanoma cells with low toxicity to healthy fibroblasts. Strahlentherapie und Onkologie : Organ der Deutschen Rontgengesellschaft ... [et al], 10.1007/s00066-022-02009-x. Advance online publication. https://doi.org/10.1007/s00066-022-02009-x
Jost, T., Schultz, A. K., Frey, B., Vu, J., Fietkau, R., Distel, L. V., & Hecht, M. (2022). Influence of alectinib and crizotinib on ionizing radiation - in vitro analysis of ALK/ROS1-wildtype lung tissue cells. Neoplasia (New York, N.Y.), 27, 100780. https://doi.org/10.1016/j.neo.2022.100780
Weitere Publikationen von Dr. Tina Jost verfügbar unter der "Web of Sciences Researcher ID".
Kooperationspartner
Prof. Dr. Cornelia Brunner
Akademische Oberrätin, Wissenschaftliche Leitung des Forschungslabors, Klinik für Hals-Nasen-Ohrenheilkunde, Kopf- und Halschirurgie, Universitätsklinik Ulm, Deutschland
Prof. Dr. Andriy Mokhir
Professur für Organische Chemie, Department Chemie und Pharmazie, Friedrich-Alexander Universität Erlangen-Nürnberg, Erlangen, Deutschland
Projekt-relevante eingeworbene Drittmittel
DFG Förderung:
ab 01.01.2026:
Projekt: „Molekulare Mechanismen der synergistischen Effekte von Strahlentherapie, ATR Inhibition und Hemmung verschiedener Immun-Checkpoints zur Verstärkung der Immunantwort bei HNSCC"